Chi1 - Classification périodique
Description
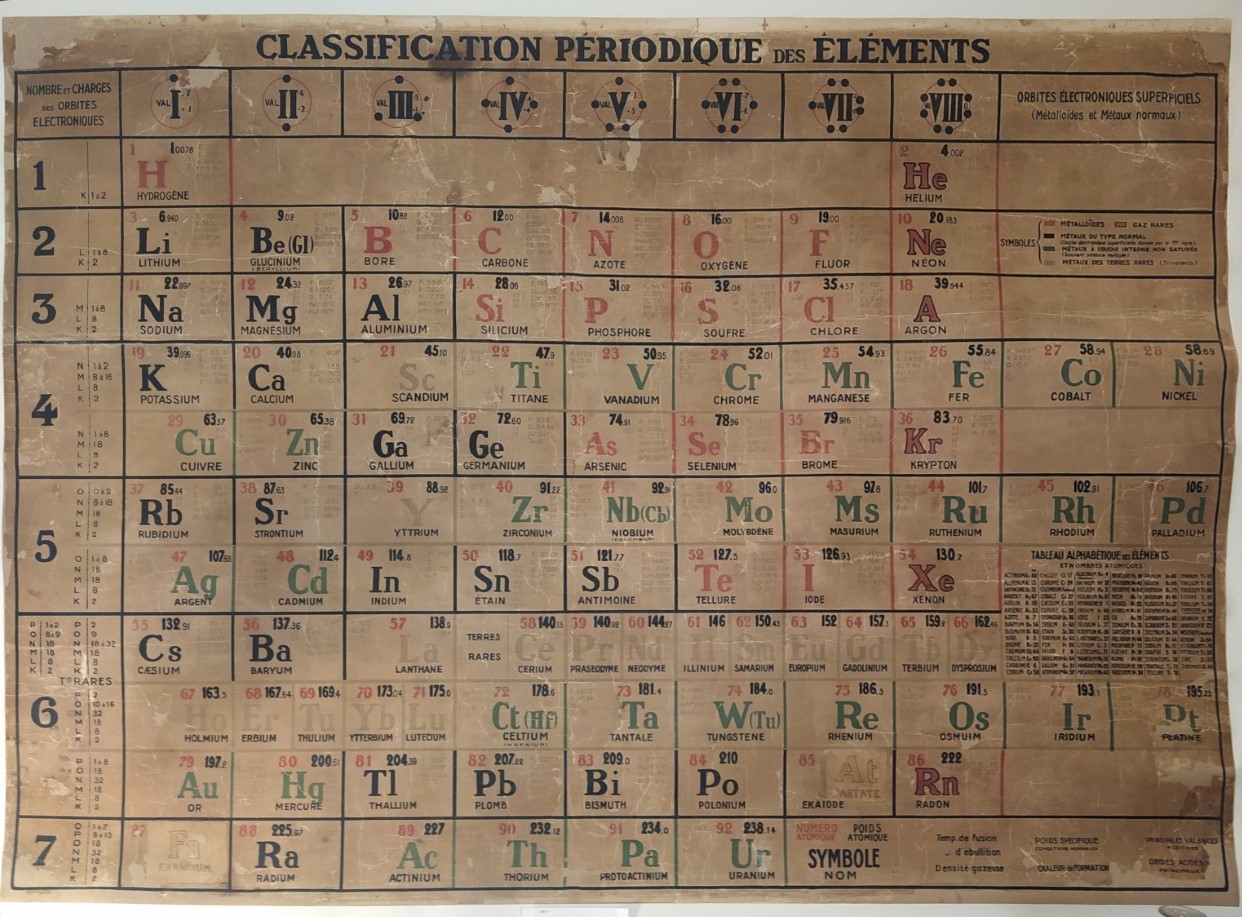
Ce tableau n'est pas très ancien, Pierre Provost se rappelle l'avoir vu sur un mur d'amphithéâtre en 1958 et se souvient de l'avoir utilisé. On remarquera que les éléments y sont classés par ordre croissant de numéro atomique (Z) et non par ordre croissant de masse atomique comme au temps de Mendeleïev ; les orbites électroniques y sont figurées. Cette classification est donc postérieure aux travaux de Henry Moseley (1887-1915).
Mais un des intérêts historiques et muséographiques de cet objet réside dans le fait que lorsqu'elle fut achetée cette classification possédait encore deux cases vides correspondant aux éléments 85 qu'on appelait (selon Mendeleïev) ékaiode (appellation encore visible) et 87 qu'on appelait ékacaesium (appellation recouverte).
L'ékacaesium fut découvert en 1939 par Mlle Marguerite Perey et nommé Francium (Fr), l'ékaiode fut découvert en 1940 par Dale Corson, Kenneth MacKensie et Emilio Segré et fut nommé Astate (At). Cet objet fut donc acheté avant la deuxième guerre mondiale.
Consciencieusement des professeurs du lycée Louis le Grand ont comblé les deux cases vides par les symboles des deux éléments découverts après l'achat. On notera cependant l'absence de transuraniens (Z>92).
Par ailleurs, on remarque que l’élément 43 s’appelle Masurium (Ms) lors de l’impression de cette classification. Or, la découverte de cet élément en 1925 par les deux chimistes allemands Ida Tacke-Noddack et Walter Noddack fut contestable et contestée. Cet élément fut véritablement découvert en 1937 et il est désormais nommé Technetium (Tc). On peut donc dater l’impression de cette classification dans la fourchette 1925-1937.

Histoire
On peut sensiblement confondre la masse atomique exprimée en grammes avec le nombre A de nucléons contenus dans l'atome. On a très vite songé à classer les éléments par ordre de masses atomiques croissantes : des périodicités apparaissent alors pour les propriétés physiques et chimiques. Plusieurs chimistes ont proposé de telles classifications : « vis tellurique » de Alexandre-Émile Chancourtois en 1862, table de John Newlands (1863-1866), mais ils ne purent pas imposer leurs vues. C'est Dimitri Ivanovitch Mendeleïev (1834-1907) chimiste Russe qui, en 1869, sut tirer tout le parti de cette classification, n'hésitant pas à laisser des cases vides (éka...) en prévoyant la découverte des éléments correspondants, et les propriétés de ces éléments. Certains furent découverts de son vivant : Gallium (Ga) par Paul-Émile Lecoq de Boisbaudran en 1875, Scandium (Sc) par Lars Nilson en 1879 et Germanium (Ge) en 1876 par Clemens Winkler. Il serait juste de dire que Lothar Meyer, en Suisse publiait en 1870 une classification presque identique à celle de Mendeleïev et qu'il l'enseignait depuis plusieurs années.
Certains éléments ne se plaçant pas de façon satisfaisante Mendeleïev suggère qu'il y avait peut-être eu erreur dans la détermination, de leurs masses atomiques. Cela fut vérifié pour certains d'entre eux (Yt, In, Di, Ce, Er, La, Tr, U). Mais Mendeleïev dut faire des entorses au principe de classification (voir tableau) : A 39,944 placé avant K 39,096, Co 58,94 avant Ni 58,69, Te 127,5 avant I 126,93.
C'est à la suite des travaux du physicien anglais Moseley (1887-1915) qui étudia le spectre des rayons X émis par les éléments, spectre caractéristique qui permet l'identification de ces éléments, que l'on comprit que c'est le nombre Z, numéro atomique, nombre de protons, donc d'électrons qui devait servir à classer les éléments et non leur masse atomique (sensiblement égale à A). C'est parce que le rapport A/Z est voisin de 2 et varie lentement pour Z croissant que le principe de classification de Mendeleïev "marchait" assez bien.